
Absorción de HCL
Recuperación eficiente y segura de cloruro de hidrógeno
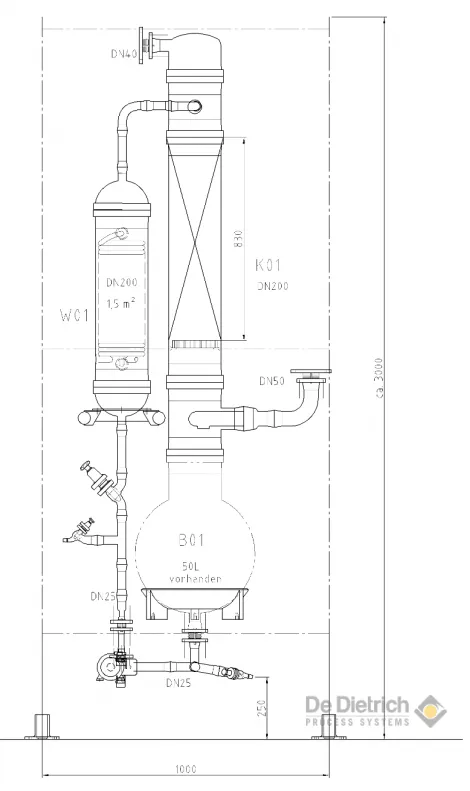
Depuración optimizada de gas HCl y recuperación de ácido
La absorción de cloruro de hidrógeno (HCl) es esencial para el tratamiento de gases residuales y la producción de ácido clorhídrico. De Dietrich ofrece sistemas de absorción de HCl de alta eficiencia que garantizan el cumplimiento ambiental, la optimización del proceso y la seguridad operativa. Nuestras soluciones incluyen depuradores, unidades de neutralización y sistemas de producción de HCl de alta pureza para diversas industrias.
Rendimiento y seguridad
Depuración de gas altamente eficiente – Garantiza el cumplimiento de estrictos estándares de emisión
Absorción segura y controlada – Maneja gases corrosivos con una selección optimizada de materiales
Soluciones diseñadas a medida – Adaptadas para cumplir con los requisitos específicos del proceso
Sistemas escalables – Desde la neutralización a pequeña escala hasta la recuperación industrial de ácido
Recuperación de ácido clorhídrico de alta pureza
Nuestros sistemas de absorción de última generación permiten la recuperación eficiente del gas HCl, convirtiéndolo en ácido clorhídrico de diversas concentraciones. Al utilizar vidrio borosilicato y acero revestido de vidrio, nuestras plantas ofrecen máxima resistencia a la corrosión, asegurando una fiabilidad a largo plazo en entornos químicos exigentes.
Aplicaciones clave
Depuración de gases residuales en plantas químicas – Reducción de emisiones de HCl para cumplir con los estándares ambientales
Recuperación de ácido clorhídrico de procesos industriales – Reutilización de HCl en las líneas de producción
Producción de HCl de alta pureza – Para aplicaciones en la industria alimentaria, farmacéutica y electrónica
Neutralización y tratamiento de corrientes de desechos ácidos – Manejo seguro y controlado de efluentes peligrosos
Soluciones personalizadas para cada industria
Nuestras tecnologías de absorción de HCl se pueden adaptar tanto para procesos por lotes como continuos, ofreciendo soluciones que reducen los costos operativos, minimizan el impacto ambiental y mejoran la eficiencia de producción. Ya sea que necesite depuración, neutralización o recuperación de ácido, diseñamos e instalamos sistemas a medida para satisfacer sus necesidades.
¿Busca un sistema de absorción de HCl eficiente y confiable?
Descargue el documento
Solicitar una descarga
Con el fin de procesar su solicitud de folleto de manera eficiente, le rogamos que nos facilite la información requerida a través de nuestro formulario.